Ο Karin δήλωσε ότι οι ερευνητές θα ήθελαν να αναπτύξουν περαιτέρω το Ε7 ως κλινικά χρήσιμη εναλλακτική λύση στην ινσουλίνη "επειδή έχουμε κάθε λόγο να πιστεύουμε ότι είναι απίθανο να προκαλέσει σοκ ινσουλίνης"
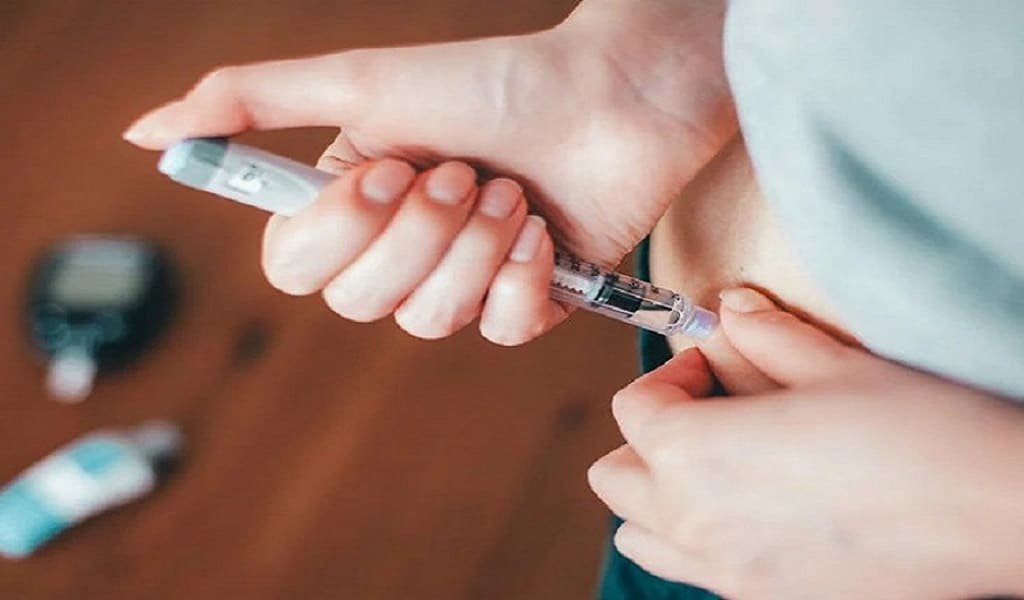
Ινσουλίνη: Έχει περάσει λίγο περισσότερο από ένας αιώνας από την ανακάλυψη της ινσουλίνης, μια χρονική περίοδος κατά την οποία οι θεραπευτικές δυνάμεις της ορμόνης έχουν διευρυνθεί και τελειοποιηθεί. Η ινσουλίνη αποτελεί βασική θεραπεία για τον διαβήτη τύπου 1 και συχνά και για τον διαβήτη τύπου 2. Περίπου 8,4 εκατομμύρια Αμερικανοί χρησιμοποιούν ινσουλίνη, σύμφωνα με την Αμερικανική Ένωση Διαβήτη. Εκατό χρόνια έρευνας έχουν προχωρήσει σημαντικά την ιατρική και βιοχημική κατανόηση του πώς λειτουργεί η ινσουλίνη και τι συμβαίνει όταν λείπει, αλλά το αντίστροφο, το πώς προλαμβάνεται η δυνητικά θανατηφόρα υπεραντιδραστικότητα της ινσουλίνης, παραμένει ένα επίμονο μυστήριο.

Σε μια νέα μελέτη, που δημοσιεύεται στην ηλεκτρονική έκδοση της 20ής Απριλίου 2023 του Cell Metabolism, μια ομάδα επιστημόνων της Ιατρικής Σχολής του Πανεπιστημίου της Καλιφόρνια στο Σαν Ντιέγκο, μαζί με συναδέλφους τους αλλού, περιγράφουν έναν παίκτη-κλειδί στον αμυντικό μηχανισμό που μας προστατεύει από την υπερβολική ινσουλίνη στο σώμα. “Αν και η ινσουλίνη είναι μία από τις πιο βασικές ορμόνες, η ανεπάρκεια της οποίας μπορεί να οδηγήσει σε θάνατο, η υπερβολική ινσουλίνη μπορεί επίσης να είναι θανατηφόρα”, δήλωσε ο επικεφαλής συγγραφέας της μελέτης Michael Karin, Ph.D., διακεκριμένος καθηγητής Φαρμακολογίας και Παθολογίας στην Ιατρική Σχολή του UC San Diego. “Ενώ ο οργανισμός μας συντονίζει με λεπτό τρόπο την παραγωγή ινσουλίνης, οι ασθενείς που υποβάλλονται σε θεραπεία με ινσουλίνη ή φάρμακα που διεγείρουν την έκκριση ινσουλίνης εμφανίζουν συχνά υπογλυκαιμία, μια κατάσταση που αν δεν αναγνωριστεί και δεν αντιμετωπιστεί μπορεί να οδηγήσει σε επιληπτικές κρίσεις, κώμα και ακόμη και θάνατο, τα οποία συνολικά ορίζουν μια κατάσταση που ονομάζεται ινσουλινοσόκ”. Η υπογλυκαιμία (χαμηλό σάκχαρο στο αίμα) αποτελεί σημαντική αιτία θανάτου μεταξύ των ατόμων με διαβήτη. Στη νέα μελέτη, ο Karin, η πρώτη συγγραφέας Li Gu, Ph.D., μεταδιδακτορική ερευνήτρια στο εργαστήριο του Karin, και οι συνεργάτες της περιγράφουν “τη φυσική άμυνα ή βαλβίδα ασφαλείας του οργανισμού” που μειώνει τον κίνδυνο του σοκ ινσουλίνης.
Αυτή η βαλβίδα είναι ένα μεταβολικό ένζυμο που ονομάζεται φωσφατάση της φρουκτόζης-1,6-διφωσφορικής ή FBP1, το οποίο δρα για να ελέγχει τη γλυκονεογένεση, μια διαδικασία κατά την οποία το ήπαρ συνθέτει γλυκόζη (την πρωταρχική πηγή ενέργειας που χρησιμοποιείται από τα κύτταρα και τους ιστούς) κατά τη διάρκεια του ύπνου και την εκκρίνει για να διατηρήσει σταθερή παροχή γλυκόζης στην κυκλοφορία του αίματος. Ορισμένα αντιδιαβητικά φάρμακα, όπως η μετφορμίνη, αναστέλλουν τη γλυκονεογένεση αλλά χωρίς εμφανή αρνητική επίδραση. Τα παιδιά που γεννιούνται με μια σπάνια, γενετική διαταραχή κατά την οποία δεν παράγουν επαρκές μεταβολικό ένζυμο FBP1 μπορούν επίσης να παραμείνουν υγιή και να ζήσουν μακροχρόνια. Αλλά σε άλλες περιπτώσεις, όταν ο οργανισμός λιμοκτονεί για γλυκόζη ή υδατάνθρακες, μια ανεπάρκεια του ενζύμου FBP1 μπορεί να οδηγήσει σε σοβαρή υπογλυκαιμία. Χωρίς έγχυση γλυκόζης, μπορεί να προκληθούν σπασμοί, κώμα και ενδεχομένως θάνατος.
Συμπληρώνοντας και επιδεινώνοντας το πρόβλημα, η ανεπάρκεια του μεταβολικού ενζύμου FPB1 σε συνδυασμό με την πείνα για γλυκόζη προκαλεί ανεπιθύμητες ενέργειες που δεν σχετίζονται με τη γλυκονεογένεση, όπως ένα διογκωμένο, λιπώδες ήπαρ, ήπια ηπατική βλάβη και αυξημένα λιπίδια ή λίπη στο αίμα. Για την καλύτερη κατανόηση του ρόλου του ενζύμου FBP1, οι ερευνητές δημιούργησαν ένα μοντέλο ποντικού με ειδική ανεπάρκεια του μεταβολικού ενζύμου FBP1 στο ήπαρ, μιμούμενοι με ακρίβεια την ανθρώπινη κατάσταση. Όπως και τα παιδιά με ανεπάρκεια του μεταβολικού ενζύμου FBP1, τα ποντίκια φαίνονταν φυσιολογικά και υγιή μέχρι να νηστέψουν, γεγονός που οδήγησε γρήγορα στη σοβαρή υπογλυκαιμία και στις ηπατικές ανωμαλίες και την υπερλιπιδαιμία που περιγράφηκαν παραπάνω. Η Gu και οι συνεργάτες της ανακάλυψαν ότι το μεταβολικό ένζυμο FBP1 είχε πολλαπλούς ρόλους. Πέρα από το ότι έπαιζε ρόλο στη μετατροπή της φρουκτόζης σε γλυκόζη, το μεταβολικό ένζυμο FBP1 είχε μια δεύτερη μη ενζυμική αλλά κρίσιμη λειτουργία: Ανέστειλε την πρωτεϊνική κινάση AKT, η οποία είναι ο κύριος αγωγός της δραστηριότητας της ινσουλίνης. “Βασικά, το ένζυμο FBP1 κρατά την πρωτεϊνική κινάση AKT υπό έλεγχο και προφυλάσσει από την υπεραντιδραστικότητα στην ινσουλίνη, το υπογλυκαιμικό σοκ και την οξεία λιπώδη ηπατική νόσο”, δήλωσε η πρώτη συγγραφέας Gu.
Σε συνεργασία με τον Yahui Zhu, επιστήμονα vising από το Πανεπιστήμιο Chongqing στην Κίνα και δεύτερο συγγραφέα της μελέτης, η Gu ανέπτυξε ένα πεπτίδιο (μια σειρά αμινοξέων) που προέρχεται από το ένζυμο FBP1 και διέκοψε τη σύνδεση του ενζύμου FBP1 με την πρωτεϊνική κινάση AKT και μια άλλη πρωτεΐνη που αδρανοποιεί την πρωτεϊνική κινάση AKT. “Αυτό το πεπτίδιο λειτουργεί σαν μιμητικό της ινσουλίνης, ενεργοποιώντας την πρωτεϊνική κινάση AKT”, δήλωσε ο Karin. “Όταν χορηγείται με ένεση σε ποντίκια που έχουν καταστεί ανθεκτικά στην ινσουλίνη, μια πολύ συχνή προ-διαβητική κατάσταση, λόγω παρατεταμένης κατανάλωσης δίαιτας υψηλής περιεκτικότητας σε λιπαρά, το πεπτίδιο (με το ψευδώνυμο Ε7) μπορεί να αντιστρέψει την αντίσταση στην ινσουλίνη και να αποκαταστήσει τον φυσιολογικό γλυκαιμικό έλεγχο”. Ο Karin δήλωσε ότι οι ερευνητές θα ήθελαν να αναπτύξουν περαιτέρω το Ε7 ως κλινικά χρήσιμη εναλλακτική λύση στην ινσουλίνη “επειδή έχουμε κάθε λόγο να πιστεύουμε ότι είναι απίθανο να προκαλέσει σοκ ινσουλίνης”
Διαβάστε όλες τις τελευταίες Ειδήσεις για την υγεία από την Ελλάδα και τον ΚόσμοΑκολουθήστε το healthweb.gr στο Google News και μάθετε πρώτοι όλες τις ειδήσεις
Ακολουθήστε το healthweb.gr στο κανάλι μας στο YouTube