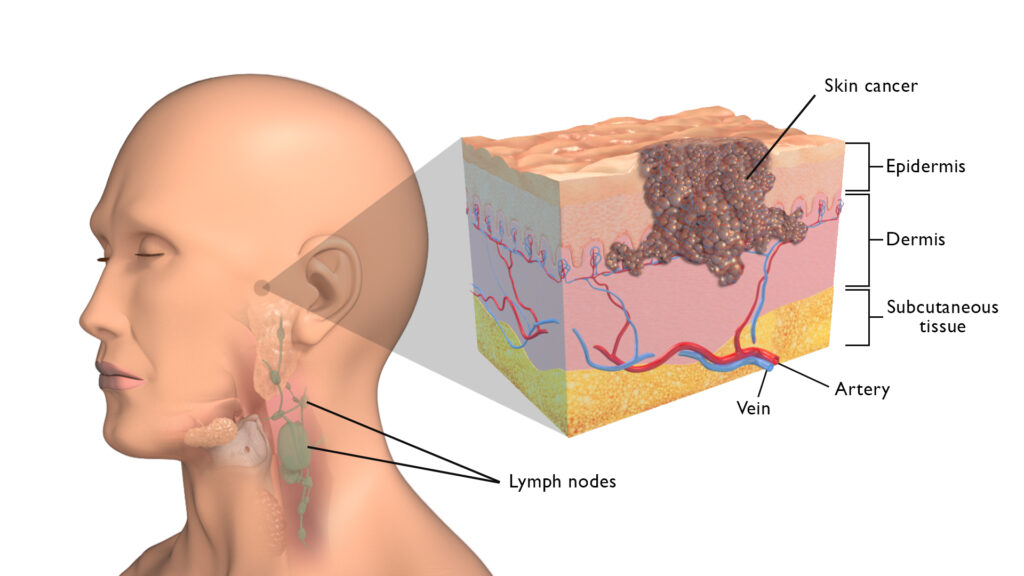
Καρκινικά κύτταρα ανοσοποιητικό: Οι επιστήμονες του Τορόντο έχουν χαρτογραφήσει τα γονίδια που επιτρέπουν στα καρκινικά κύτταρα να αποφύγουν να σκοτωθούν από το ανοσοποιητικό σύστημα σε ένα εύρημα που ανοίγει το δρόμο για την ανάπτυξη ανοσοθεραπειών που θα ήταν αποτελεσματικές για μεγαλύτερους πληθυσμούς ασθενών και σε διαφορετικούς τύπους όγκων. «Την τελευταία δεκαετία, διάφορες μορφές ανοσοθεραπείας έχουν εμφανιστεί ως πραγματικά ισχυρές θεραπείες για τον καρκίνο, αλλά η πραγματικότητα είναι ότι παράγουν ανθεκτικές απαντήσεις μόνο σε ένα κλάσμα ασθενών και όχι για όλους τους τύπους όγκων», λέει ο Jason Moffat, καθηγητής μοριακής γενετικής στο το Κέντρο Donnelly για Κυτταρική και Βιομοριακή Έρευνα στο Πανεπιστήμιο του Τορόντο, ο οποίος ηγήθηκε του έργου.
Η μελέτη αποκάλυψε επίσης την ανάγκη μιας νέας θεραπείας να λαμβάνει υπόψη τη γενετική σύνθεση των όγκων λόγω μεταλλάξεων στα καρκινικά κύτταρα που μπορεί δυνητικά να επιδεινώσουν την ασθένεια σε απόκριση στη θεραπεία, που συχνά αναφέρονται ως μεταλλάξεις αντίστασης στον καρκίνο. “Είναι πολύ σημαντικό να κατανοήσουμε σε μοριακό επίπεδο πώς ο καρκίνος αναπτύσσει αντίσταση στις ανοσοθεραπείες προκειμένου να τις καταστήσει ευρύτερα διαθέσιμες. Οι εξελίξεις στις συστηματικές γενετικές προσεγγίσεις μας επέτρεψαν να εισαγάγουμε γονίδια και μοριακές οδούς που συνήθως εμπλέκονται στην αντίσταση στη θεραπεία” λέει ο Moffat, ο οποίος είναι κάτοχος της έδρας έρευνας του Καναδά στη λειτουργική γονιδιωματική του καρκίνου. Διαβάστε επίσης: Καρκίνος θεραπεία νέα: Νέος τρόπος στόχευσης καρκινικών κυττάρων
Στην ανοσοθεραπεία, τα κύτταρα του ανοσοποιητικού ενός ασθενούς, γνωστά ως Τ δολοφονικά κύτταρα, σχεδιάστηκαν για να βρουν και να καταστρέψουν τον καρκίνο. Ωστόσο, η αντίσταση στη θεραπεία απέκλεισε τη χρήση της στους περισσότερους ασθενείς, ειδικά σε ασθενείς με συμπαγείς όγκους. “Είναι μια συνεχής μάχη μεταξύ του ανοσοποιητικού συστήματος και του καρκίνου, όπου το ανοσοποιητικό σύστημα προσπαθεί να βρει και να σκοτώσει τον καρκίνο, ενώ η δουλειά του καρκίνου είναι να αποφύγει αυτή τη δολοφονία”, λέει ο Keith Lawson, συν-επικεφαλής συγγραφέας που ολοκλήρωσε διδακτορικό. στο εργαστήριο του Moffat ως μέρος της ιατρικής του εκπαίδευσης στο Πρόγραμμα Χειρουργού-Επιστήμονα στην Ιατρική Σχολή του Τ.
Η ετερογένεια των όγκων – γενετική διακύμανση των καρκινικών κυττάρων εντός και μεταξύ ατόμων που μπορούν να επηρεάσουν την ανταπόκριση στη θεραπεία – περιπλέκει περαιτέρω τα πράγματα. “Είναι σημαντικό να μην βρίσκουμε μόνο γονίδια που μπορούν να ρυθμίσουν την αποφυγή του ανοσοποιητικού συστήματος σε ένα μοντέλο καρκίνου, αλλά αυτό που πραγματικά θέλεις είναι να βρεις εκείνα τα γονίδια που μπορείς να χειριστείς σε καρκινικά κύτταρα σε πολλά μοντέλα, επειδή αυτά θα κάνουν τους καλύτερους θεραπευτικούς στόχους, “λέει ο Lawson.
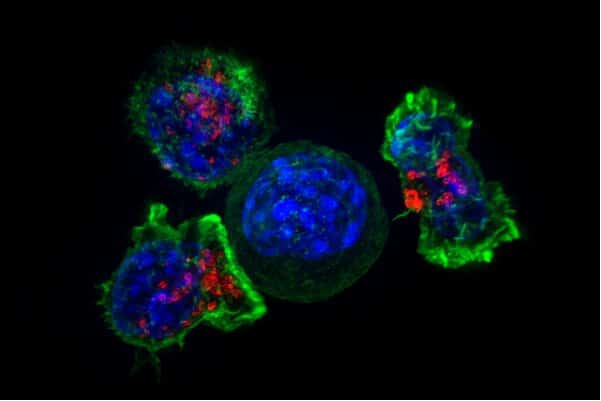
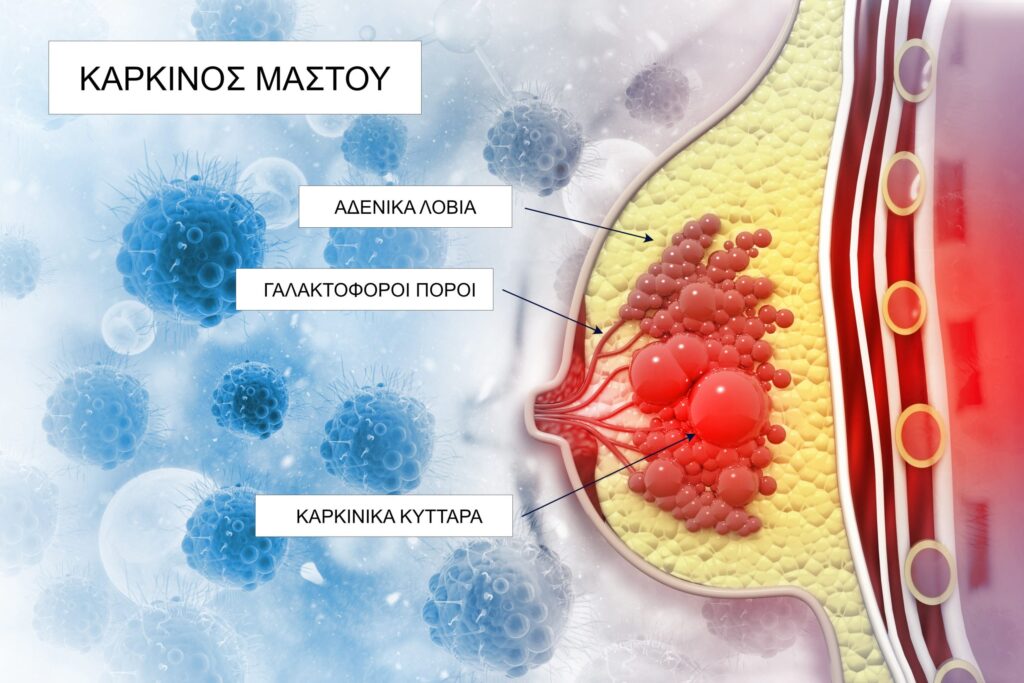
Η ομάδα, συμπεριλαμβανομένων των συνεργατών της Agios Pharmaceuticals στο Cambridge της Μασαχουσέτης, αναζήτησε γονίδια που ρυθμίζουν την ανοσοδιαφυγή σε έξι γενετικά διαφορετικά μοντέλα όγκων που προέρχονται από καρκίνο του μαστού, του παχέος εντέρου, των νεφρών και του δέρματος. Τα καρκινικά κύτταρα τοποθετήθηκαν σε ένα πιάτο δίπλα στα Τ κύτταρα που σχεδιάστηκαν για να τα σκοτώσουν, όπου η επακόλουθη επίθεση χρησίμευσε ως βασική γραμμή. Στη συνέχεια, οι ερευνητές ανέπτυξαν το εργαλείο επεξεργασίας γονιδίων CRISPR για να απενεργοποιήσουν ένα προς ένα κάθε γονίδιο στα καρκινικά κύτταρα και μέτρησαν τις προκύπτουσες αποκλίσεις από τη γραμμή θανάτωσης.
Εντοπίστηκαν 182 “γονίδια εσωτερικής ανοσοδιαφυγής καρκίνου πυρήνα” των οποίων η διαγραφή καθιστά τα κύτταρα είτε πιο ευαίσθητα είτε πιο ανθεκτικά στην επίθεση Τ κυττάρων. Μεταξύ των ανθεκτικών ήταν όλα τα γονίδια που ήταν γνωστό ότι αναπτύσσουν μεταλλάξεις σε ασθενείς που σταμάτησαν να ανταποκρίνονται στην ανοσοθεραπεία, δίνοντας στους ερευνητές την εμπιστοσύνη ότι η προσέγγισή τους λειτούργησε. Πολλά από τα γονίδια που βρέθηκαν δεν είχαν προηγούμενους δεσμούς με την αποφυγή του ανοσοποιητικού συστήματος. “Αυτό ήταν πραγματικά συναρπαστικό να το δούμε, γιατί σημαίνει ότι το σύνολο δεδομένων μας ήταν πολύ πλούσιο σε νέες βιολογικές πληροφορίες”, λέει ο Lawson. Τα γονίδια που εμπλέκονται στην αυτοφαγία, μια διαδικασία όταν τα κύτταρα αυξάνουν την ανακύκλωση των συστατικών τους για τον μετριασμό της βλάβης μετά από άγχος, εμφανίστηκαν ως κλειδί για την αποφυγή του ανοσοποιητικού συστήματος. Αυτό θέτει ένα πιθανότητα ότι ο καρκίνος επιδεκτικότητα «s σε ανοσοθεραπεία θα μπορούσε να ενισχυθεί με την στόχευση γονιδίων αυτοφαγία της.
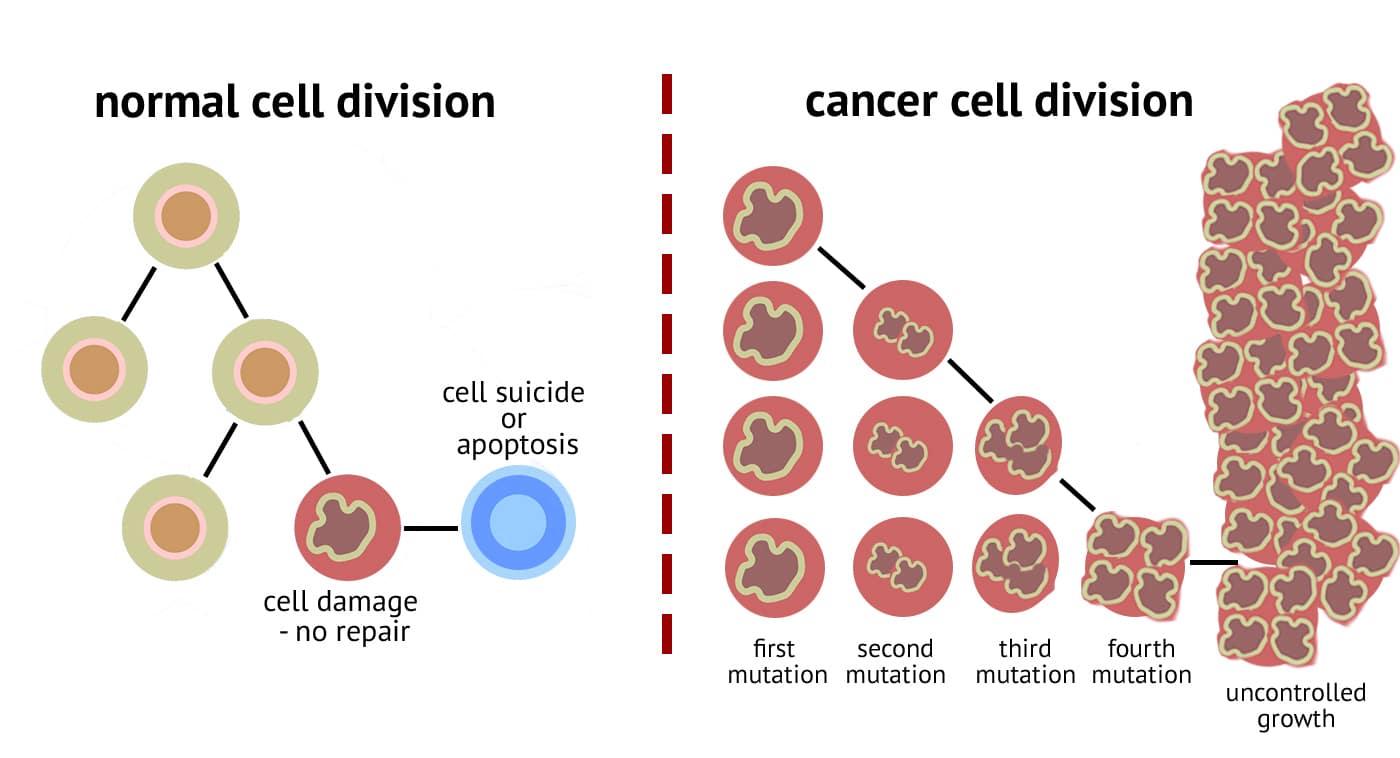
Όμως, καθώς οι ερευνητές εξερεύνησαν βαθύτερα, διαπίστωσαν ότι η διαγραφή ορισμένων γονιδίων αυτοφαγίας σε ζεύγη κατέστησε τα κύτταρα ανθεκτικά στη θανάτωση των Τ κυττάρων. Αυτό σημαίνει ότι εάν ένας όγκος φιλοξενεί ήδη μια μετάλλαξη σε ένα γονίδιο αυτοφαγίας, μια θεραπεία που συνδυάζει ανοσοθεραπεία με ένα φάρμακο που στοχεύει ένα άλλο γονίδιο αυτοφαγίας θα μπορούσε να επιδεινώσει την ασθένεια σε αυτόν τον ασθενή. “Βρήκαμε αυτήν την πλήρη αντιστροφή της γονιδιακής εξάρτησης”, λέει ο Moffat. “Αυτό δεν το προβλέψαμε καθόλου. Αυτό που μας δείχνει είναι ότι το γενετικό πλαίσιο, ποιες μεταλλάξεις υπάρχουν, υπαγορεύει πάρα πολύ εάν η εισαγωγή των δεύτερων μεταλλάξεων δεν θα προκαλέσει αποτέλεσμα, αντίσταση ή ευαισθησία στη θεραπεία”. Καθώς περισσότερη έρευνα διερευνά τις συνδυαστικές επιδράσεις των μεταλλάξεων σε διαφορετικούς τύπους καρκινικών κυττάρων , θα πρέπει να καταστεί δυνατό να προβλεφθεί από το DNA ενός όγκου ποιος τύπος θεραπείας θα είναι πιο αποτελεσματικός. Η μελέτη δημοσιεύεται στο Nature.
Διαβάστε όλες τις τελευταίες Ειδήσεις για την υγεία από την Ελλάδα και τον ΚόσμοΑκολουθήστε το healthweb.gr στο Google News και μάθετε πρώτοι όλες τις ειδήσεις
Ακολουθήστε το healthweb.gr στο κανάλι μας στο YouTube