Ερευνητές από το Πανεπιστήμιο της Καλιφόρνια Σαν Ντιέγκο έχουν εντοπίσει έναν απροσδόκητο μηχανισμό που θα μπορούσε να βοηθήσει να καθοριστεί αν ένας ασθενής με καρκίνο θα ανταποκριθεί στην ανοσοθεραπεία.
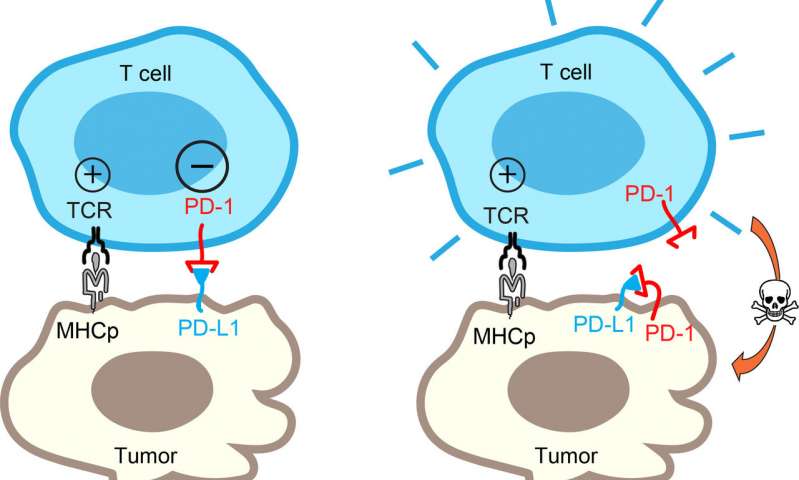
Ιδανικά, το ανοσοποιητικό σύστημα αναγνωρίζει όγκους, απειλώντας στοιχεία και αναπτύσσοντας ανοσοποιητικού κύτταρα (Τ κύτταρα) για να βρει και να τους σκοτώσει . Ωστόσο, τα καρκινικά κύτταρα έχουν εξελιχθεί για να χρησιμοποιήσουν μια πρωτεΐνη που ονομάζεται PD-L1 σε τυφλά Τ κύτταρα από την εκτέλεση των λειτουργιών τους και να αποφύγουν την ανοσολογική άμυνα. Το PD-L1 προστατεύει τα κύτταρα όγκου ενεργοποιώντας ένα “μοριακό φρένο” γνωστό ως PD-1 για να σταματήσει τα Τ κύτταρα.
Σε σημαντική θεραπευτική πρόοδο, τα αντισώματα που αναπτύχθηκαν για να εμποδίσουν την PD-L1 / PD-1 έχουν αποδειχθεί κλινικά ότι ωφελούν ορισμένους καρκινοπαθείς. Ωστόσο, γιατί μερικοί ασθενείς δεν ανταποκρίνονται σε μια τέτοια θεραπεία παρέμεινε ένα μυστήριο. Τώρα, ο Yunlong Zhao του UC San Diego, ο Enfu Hui και οι συνεργάτες του στο Πανεπιστήμιο του Σικάγου και η Ιατρική Σχολή του Nanjing στην Κίνα έχουν αποκαλύψει κάποιες ενδείξεις.
Όπως περιγράφηκε στις 10 Ιουλίου στο περιοδικό Cell Reports , οι ερευνητές ανακάλυψαν μια απροσδόκητη συστροφή στη μάχη των όγκων έναντι των κυττάρων Τ. Ορισμένα κύτταρα όγκου εμφανίζουν όχι μόνο το όπλο PD-L1, αλλά και το PD-1 “φρένο”. Αυτή η ταυτόχρονη έκφραση οδηγεί την PD-1 να δεσμεύσει και να εξουδετερώσει το PD-L1 στο ίδιο κύτταρο όγκου. Έτσι, το PD-L1 σε αυτά τα καρκινικά κύτταρα δεν μπορεί πλέον να εμπλέξει το φρένο PD-1 στα Τ κύτταρα.
“Είναι ένα πολύ συναρπαστικό εύρημα”, δήλωσε ο Hui. “Η μελέτη μας αποκάλυψε έναν απροσδόκητο ρόλο του PD-1 και μιας άλλης διάστασης της ρύθμισης PD-1 με σημαντικές θεραπευτικές συνέπειες”. Αυτή η μελέτη υποδεικνύει ότι οι ασθενείς με υψηλά επίπεδα PD-1 σε καρκινικά κύτταρα μπορεί να μην ανταποκρίνονται καλά στα αντισώματα αποκλεισμού επειδή η οδός PD-1 είναι μπερδεμένη. Σε αυτούς τους ασθενείς, μηχανισμοί εκτός από PD-L1 / PD-1 χρησιμοποιούνται πιθανώς από τους όγκους για να διαφύγουν από την καταστροφή του ανοσοποιητικού συστήματος.
Αναζητώντας την επέκταση του ανοσοθεραπευτικού δυναμικού του ευρήματος, ο Hui και οι συνάδελφοί του επιδιώκουν πλέον να προσδιορίσουν πρόσθετους μηχανισμούς “αυτοαποκλεισμού” στη διεπαφή των όγκων και των ανοσολογικών κυττάρων. “Πιστεύουμε ότι το εύρημα μας είναι η κορυφή του παγόβουνου”, δήλωσε ο Hui, ο οποίος πρόσφατα ονομάστηκε επιστημονικός συνεργάτης της Pew Biomedical και ο Searle Scholar. “Εικάζουμε ότι η αυτό-ακύρωση είναι ένας γενικός μηχανισμός για τη ρύθμιση της λειτουργίας των ανοσοκυττάρων . Η κατανόηση αυτών των διαδικασιών με μεγαλύτερη σαφήνεια θα βοηθήσει στην ανάπτυξη καλύτερων στρατηγικών ανοσοθεραπείας και θα προβλέπει πιο αξιόπιστα αν ο ασθενής θα ανταποκριθεί ή όχι.