Νέα θεραπεία της Novartis λαμβάνει έγκριση από τον FDA για το προσφέροντας στους ασθενείς με υγρού τύπου ΗΕΩ κέρδος στην οπτική οξύτητα και μεγαλύτερη μείωση του υγρού σε σύγκριση με την αφλιμπερσέπτη
Σε δύο κλινικές μελέτες άμεσης σύγκρισης (head-to-head), οι ασθενείς στο σκέλος θεραπείας με brolucizumab πέτυχαν τον πρώτο χρόνο βελτίωση στο κέρδος της οπτικής οξύτητας μη κατώτερο από αυτό της αφλιμπερσέπτης, με μεγαλύτερα μεσοδιαστήματα θεραπείας στην πλειονότητα των ασθενών.Το brolucizumab επέδειξε μεγαλύτερες μειώσεις στο πάχος του κεντρικού υποπεδίου (CST- ένας βασικός δείκτης παρουσίας υγρού στον αμφιβληστροειδή) ήδη από την εβδομάδα 16 και τον πρώτο χρόνο, συγκριτικά με την αφλιμπερσέπτη.
Το brolucizumab είναι ο μόνος αντι-VEGF παράγοντας για την υγρού τύπου ΗΕΩ, ο οποίος συστήνεται για να διατηρήσει ασθενείς που πληρούν τα κριτήρια σε θεραπεία με μεσοδιαστήματα έως και τριών μηνών αμέσως μετά τη φάση φόρτισης, χωρίς κανέναν συμβιβασμό ως προς την αποτελεσματικότητα. Και στις δύο κλινικές μελέτες, το χρόνο 1, περισσότεροι από τους μισούς ασθενείς παρέμειναν σε θεραπεία με μεσοδιάστημα τριών μηνών (56% στη HAWK και 51% στη HARRIER)1,2
Τα μικρά μεσοδιαστήματα έγχυσης είναι ένα συχνό αίτιο διακοπής της θεραπείας σε ασθενείς με υγρή ηλικιακή εκφύλιση της ωχράς κηλίδας (ΗΕΩ), η οποία αποτελεί μια κύρια αιτία τύφλωσης, προσβάλλοντας περισσότερους από 20 εκατομμύρια ανθρώπους παγκοσμίως3-5
Η Novartis ανακοίνωσε ότι ο Οργανισμός Ελέγχου Φαρμάκων και Τροφίμων (FDA) των ΗΠΑ ενέκρινε το brolucizumab, γνωστό και ως RTH258, για τη θεραπεία της υγρού τύπου ηλικιακής εκφύλισης της ωχράς κηλίδας (ΗΕΩ)1. Το brolucizumab είναι ο πρώτος εγκεκριμένος από τον FDA αντι-VEGF παράγοντας, ο οποίος εξασφαλίζει τόσο τη μεγαλύτερη μείωση του υγρού σε σύγκριση με την αφλιμπερσέπτη όσο και επιτρέπει,σε ασθενείς με υγρή ΗΕΩ που πληρούν τα κριτήρια, να παραμείνουν σε σκέλος θεραπείας ανά τρίμηνο, αμέσως μετά τη φάση φόρτισης διάρκειας τριών μηνών1, χωρίς κανένα συμβιβασμό ως προς την αποτελεσματικότητα.

«Το brolucizumab επιτυγχάνει τους στόχους μας στην κλινική πράξη για τη θεραπεία της υγρού τύπου ΗΕΩ: βελτίωση της όρασης και «στέγνωμα» του υγρού του αμφιβληστροειδή», ανέφερε ο Δρ Pravin U. Dugel, Διευθύνων Εταίρος της «Retinal Consultants of Arizona», Κλινικός Καθηγητής στο Οφθαλμολογικό Ινστιτούτο Roski της Ιατρικής Σχολής Keck (Πανεπιστήμιο Νότιας Καλιφόρνιας) και κύριος ερευνητής της κλινικής μελέτης HAWK. «Με το brolucizumab, η μεγαλύτερη μείωση του υγρού φάνηκε από τις μεγαλύτερες μειώσεις στο πάχος του αμφιβληστροειδούς και το μεγαλύτερο ποσοστό ασθενών με πιο στεγνό αμφιβληστροειδή. Σε συνδυασμό με τη δυνατότητα έγχυσης στους ασθενείς ανά τρεις μήνες, η έγκριση αυτή μπορεί να αλλάξει τον τρόπο που προσεγγίζουμε τη θεραπεία της υγρής ΗΕΩ.»
Η έγκριση του brolucizumab βασίστηκε σε ευρήματα των φάσης ΙΙΙ κλινικών μελετών HAWK και HARRIER, σύμφωνα με τις οποίες το brolucizumab επέδειξε μη κατωτερότητα έναντι της αφλιμπερσέπτης ως προς τη μέση μεταβολή της καλύτερα διορθωμένης οπτικής οξύτητας (BCVA) τον χρόνο 1 (εβδομάδα 48)1,2.
Και στις δύο κλινικές δοκιμές, περίπου 30% των ασθενών κέρδισαν τουλάχιστον 15 γράμματα τον χρόνο 11,2. Στις κλινικές δοκιμές HAWK και HARRIER παρατηρήθηκε μεγαλύτερη μείωση του πάχους κεντρικού υποπεδίου (CST) ήδη από την εβδομάδα 16 και στον χρόνο 1 στους ασθενείς που λάμβαναν brolucizumab, ενώ λιγότεροι ασθενείς είχαν ενδοαμφιβληστροειδικό (IRF) ή/και υποαμφιβληστροειδικό υγρό (SRF),2. Το υγρό στον αμφιβληστροειδή χιτώνα είναι βασικός δείκτης ενεργότητας της νόσου.
Η υγρή ΗΕΩ είναι μια χρόνια, εκφυλιστική οφθαλμική νόσος που προκαλείται από περίσσεια του VEGF, μιας πρωτεΐνης που προάγει την αύξηση παθολογικών αιμοφόρων αγγείων κάτω από την ωχρά κηλίδα, την περιοχή του αμφιβληστροειδούς που είναι υπεύθυνη για την οξεία, κεντρική όραση7,8. Η διαρροή υγρού από αυτά τα παθολογικά αιμοφόρα αγγεία διαταράσσει τη φυσιολογική δομή του αμφιβληστροειδούς και τελικά καταστρέφει την ωχρά κηλίδα8-10. Το μόριο brolucizumab είναι κατάλληλα κατασκευασμένο ώστε να αποδίδει την υψηλότερη συγκέντρωση του φαρμάκου, παρέχοντας πιο δραστικούς παράγοντες πρόσδεσης σε σύγκριση με άλλους αντι-VEGF παράγοντες2. Με την αναστολή του VEGF, το brolucizumab καταστέλλει την αύξηση των παθολογικών αιμοφόρων αγγείων και τη δυνητική διαρροή υγρού στον αμφιβληστροειδή 2.
Η Marie-France Tschudin, Πρόεδρος της Novartis Pharmaceuticals, δήλωσε: «Η έγκριση του brolucizumab συμβάλει στη δέσμευση της Novartis στον επαναπροσδιορισμό των θεραπειών ασθενών που πάσχουν από σοβαρή έκπτωση της όρασης. Στις επισημάνσεις των υπαρχουσών θεραπειών αναφέρεται ότι δεν είναι τόσο δραστικά όταν χορηγούνται κάθε 12 εβδομάδες. Το brolucizumab είναι το πρώτο προϊόν που προσφέρει λιγότερο συχνή χορήγηση τον πρώτο χρόνο, ενώ παράλληλα διατηρεί την αποτελεσματικότητά του. Αυτό επιτρέπει στους ασθενείς με υγρή ΗΕΩ να έχουν περισσότερο χρόνο για να επικεντρωθούν σε ό,τι είναι σημαντικό για αυτούς στη ζωή τους.»
Στις κλινικές μελέτες HAWK και HARRIER, οι ασθενείς που πληρούσαν τα κριτήρια μπορούσαν να παραμείνουν σε μεσοδιάστημα θεραπείας κάθε τρεις μήνες, , αμέσως μετά τη φάση φόρτισης 1,2. Τον χρόνο 1, περισσότεροι από τους μισούς ασθενείς παρέμειναν σε μεσοδιάστημα θεραπείας κάθε τρεις μήνες (56% στη HAWK και 51% στη HARRIER)1,2 Οι υπόλοιποι ασθενείς της μελέτης θεραπεύονταν ανά χρονικό διάστημα δύο μηνών1,2.
Το προφίλ ασφάλειας του brolucizumab ήταν συγκρίσιμο με αυτό της αφλιμπερσέπτης. Το brolucizumab αντενδείκνυται σε ασθενείς με οφθαλμικές ή περιοφθαλμικές λοιμώξεις, ενεργή ενδοφθάλμια φλεγμονή ή γνωστή υπερευαισθησία στο brolucizumab ή σε οποιοδήποτε έκδοχο1. Οι αντιδράσεις υπερευαισθησίας μπορεί να εκδηλωθούν ως εξάνθημα, κνησμός, κνίδωση, ερύθημα ή βαριά ενδοφθάλμια φλεγμονή1.
Τα πιο συχνά ανεπιθύμητα συμβάντα (≥5% των ασθενών) σε ασθενείς που λάμβαναν brolucizumab ήταν το θάμβος όρασης, ο καταρράκτης, η αιμορραγία επιπεφυκότα, οι μυοψίες και ο οφθαλμικός πόνος1,2.
Η υγρή ΗΕΩ παραμορφώνει την κεντρική όραση και τελικά προκαλεί τύφλωση και απώλεια της ανεξαρτησίας11,12. Υπολογίζεται ότι το 2020 1,75 εκατομμύρια άνθρωποι στις ΗΠΑ θα ζούνε με υγρή ΗΕΩ13-15, καθιστώντας την μια αυξανόμενη παράμετρο ανησυχίας για τη δημόσια υγεία. Πρώιμα συμπτώματα της υγρής ΗΕΩ είναι το θάμβος όρασης ή η μεταμορφοψία8. Καθώς η νόσος εξελίσσεται, οι ασθενείς χάνουν την κεντρική τους όραση και έτσι γίνεται δύσκολο να βλέπουν αντικείμενα που βρίσκονται ακριβώς μπροστά τους8.
Σύμφωνα με τον Dawn Prall, ιδρυτή και εκτελεστικό διευθυντή του Ιδρύματος Support Sight Foundation: «Καθώς χάνεται η όραση, ο ασθενής χάνει και την επαφή του με τον κόσμο. Καλωσορίζουμε μια νέα θεραπεία που συμβάλλει στη διατήρηση της όρασης και μπορεί να χορηγείται κάθε τρεις μήνες, κάτι που μπορεί να μειώσει το βάρος του φορτίου της νόσου των ασθενών και των φροντιστών τους, και να βοηθήσει τους ασθενείς με υγρή ΗΕΩ να συνεχίσουν να κάνουν αυτά που αγαπούν με τους ανθρώπους που αγαπούν.»
Με την έγκριση αυτή, η Novartis προσφέρει στις ΗΠΑ το πρόγραμμα Your Way™. Το πρόγραμμα αυτό παρέχει εξατομικευμένη ατομική υποστήριξη σε ασθενείς και φροντιστές, με πρόσβαση σε ειδικούς στη φροντίδα, οι οποίοι είναι αφοσιωμένοι στην κατανόηση των μοναδικών αναγκών και επιθυμιών κάθε ασθενούς. Στη Novartis είμαστε περήφανοι που συνεργαζόμαστε με οργανισμούς συνηγορίας ασθενών προκειμένου να παρέχουμε στους ασθενείς και στους φροντιστές εκπαιδευτικό υλικό. Στόχος μας είναι η ενίσχυση των ασθενών με υγρή ΗΕΩ, ώστε να ζουν ασφαλείς και ανεξάρτητοι.
Σχετικά με το brolucizumab
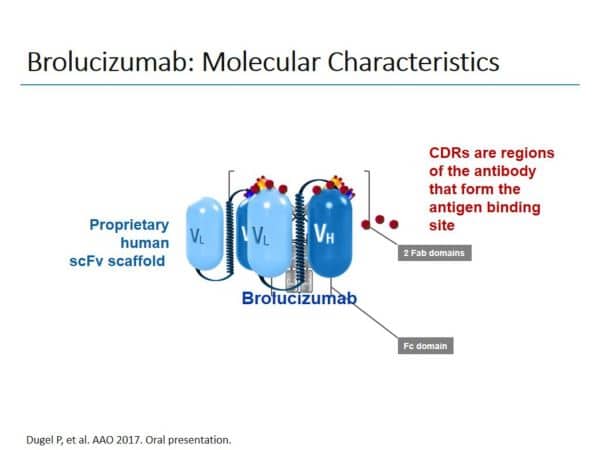
Το brolucizumab είναι το πιο κλινικά προηγμένο ανθρωποποιημένο τμήμα αντισώματος μονής αλύσου (scFv)2,16. Τα τμήματα αντισώματος μονής αλύσου είναι περιζήτητα στην ανάπτυξη φαρμάκων, λόγω μικρού μεγέθους, ενισχυμένης διεισδυτικότητάς στους ιστούς, ταχείας κάθαρσης από τη συστημική κυκλοφορία και των χαρακτηριστικών απόδοσης φαρμάκου16-18.
Η κατοχυρωμένη καινοτόμα δομή επιτρέπει τη δημιουργία ένα μικρού μορίου (26 kDa) με ισχυρή ανασταλτική δράση και υψηλή συγγένεια με όλες τις ισομορφές του VEGF-A, 17. Το brolucizumab είναι κατάλληλα κατασκευασμένο ώστε να αποδίδει την υψηλότερη συγκέντρωση του φαρμάκου, παρέχοντας πιο δραστικούς παράγοντες πρόσδεσης σε σύγκριση με άλλους αντι-VEGF παράγοντες2,16. Σε προκλινικές μελέτες, το brolucizumab ανέστειλε την ενεργοποίηση των υποδοχέων του VEGF, μέσω παρεμπόδισης της αλληλεπίδρασης συνδέτη-υποδοχέα17-19. Η αυξημένη σηματοδότηση μέσω του μονοπατιού του VEGF σχετίζεται με παθολογική οφθαλμική αγγειογένεση και οίδημα του αμφιβληστροειδούς 20. Έχει καταδειχθεί ότι η αναστολή του μονοπατιού του VEGF αναστέλλει την αύξηση των νεοαγγειακών βλαβών και καταστέλλει τον πολλαπλασιασμό των ενδοθηλιακών κυττάρων και την αγγειακή διαπερατότητα20.
Σχετικά με τις μελέτες HAWK και HARRIER
Με περισσότερους από 1.800 ασθενείς σε σχεδόν 400 κέντρα παγκοσμίως, οι μελέτες HAWK (NCT02307682) και HARRIER (NCT02434328) είναι οι πρώτες και μοναδικές παγκοσμίου επιπέδου μελέτες άμεσης σύγκρισης (head-to-head) σε ασθενείς με υγρή ΗΕΩ, οποίες προοπτικά κατέδειξαν αποτελεσματικότητα την εβδομάδα 48, εφαρμόζοντας ένα καινοτόμο δοσολογικό σχήμα q12w/q8w, με την πλειονότητα των ασθενών να στο σχήμα q12w αμέσως μετά τη φάση φόρτισης2. Και οι δύο μελέτες είναι διπλά τυφλές, προοπτικές, τυχαιοποιημένες, πολυκεντρικές, διάρκειας 96 εβδομάδων και αποτελούν μέρος της κλινικής ανάπτυξης φάσης ΙΙΙ του brolucizumab 2. Οι μελέτες ήταν σχεδιασμένες για να συγκρίνουν τη δραστικότητας και την ασφάλειας των ενδοΰαλοειδικών εγχύσεων 6 mg (HAWK και HARRIER) και 3 mg (μόνο στη HAWK) brolucizumab με τις ενδοΰαλοειδικές εγχύσεις 2 mg αφλιμπερσέπτης σε ασθενείς με υγρή ΗΕΩ2.
Σχετικά με την υγρή ηλικιακή εκφύλιση της ωχράς κηλίδας
Η υγρή ΗΕΩ αποτελεί την βασική αιτία σοβαρής έκπτωσης της όρασης και νομικής τύφλωσης σε ανθρώπους ηλικίας μεγαλύτερης των 65 ετών σε Βόρεια Αμερική, Ευρώπη, Αυστραλία και Ασία. Εκτιμάται ότι προσβάλλει 20 εκατομμύρια ανθρώπους παγκοσμίως4,5,11. Υπολογίζεται ότι το 2020 1,75 εκατομμύρια άνθρωποι στις ΗΠΑ θα πάσχουν από υγρή ΗΕΩ13-15. Υγρή ΗΕΩ εμφανίζεται όταν σχηματίζονται παθολογικά αιμοφόρα αγγεία κάτω από την ωχρά κηλίδα, την περιοχή του αμφιβληστροειδούς που είναι υπεύθυνη για την οξεία, κεντρική όραση8-10. Τα αγγεία αυτά είναι εύθρυπτα και διαρρέουν υγρό , διαταράσσοντας τη φυσιολογική αρχιτεκτονική του αμφιβληστροειδούς και τελικά προκαλούν βλάβη στην ωχρά κηλίδα8-10.
Πρώιμα συμπτώματα σε ασθενείς με υγρή ΗΕΩ είναι η παραμορφωμένη όραση (μεταμορφοψία) και η δυσκολία να βλέπουν τα αντικείμενα καθαρά8,21. Ουσιώδης είναι η έγκαιρη διάγνωση και παρέμβαση10. Καθώς η νόσος εξελίσσεται, η κυτταρική βλάβη αυξάνεται, μειώνοντας περαιτέρω την ποιότητα της όρασης8. Η εξέλιξη αυτή μπορεί να οδηγήσει σε πλήρη απώλεια της κεντρικής όρασης, καθιστώντας τον ασθενή ανίκανο να διαβάζει, να οδηγεί ή να αναγνωρίζει οικεία πρόσωπα και οδηγώντας δυνητικά στην απώλεια της ανεξαρτησίας του8,12. Χωρίς θεραπεία, η όραση μπορεί να χειροτερεύσει ταχέως 22.
Novartis και οφθαλμολογία
Στόχος μας στη Novartis είναι να ανακαλύψουμε νέους τρόπους βελτίωσης και παράτασης της ζωής των ανθρώπων. Στο πεδίο της οφθαλμολογίας, βασιζόμενοι σε δεδομένα και μετασχηματιστικές τεχνολογίες, αναπτύσσουμε και διαθέτουμε φαρμακευτικά προϊόντα και θεραπείες που αλλάζουν τη ζωή των ασθενών για νοσήματα και παθήσεις δομών του οφθαλμού από το βυθό έως το πρόσθιο ημιμόριο. Οι λύσεις στο πεδίο της οφθαλμολογίας φτάνουν σε περισσότερους από 150 εκατομμύρια ανθρώπους ετησίως, από πρόωρα βρέφη μέχρι ηλικιωμένους.
Διαβάστε όλες τις τελευταίες Ειδήσεις για την υγεία από την Ελλάδα και τον ΚόσμοΑκολουθήστε το healthweb.gr στο Google News και μάθετε πρώτοι όλες τις ειδήσεις
Ακολουθήστε το healthweb.gr στο κανάλι μας στο YouTube