ΗΠΑ FDA: Ο Αμερικανικός Οργανισμός Τροφίμων και Φαρμάκων (FDA) ενέκρινε τον βιολογικό παράγοντα spesolimab (Spevigo) για τη θεραπεία των εξάρσεων σε ενήλικες με γενικευμένη φλυκταινώδη ψωρίαση (GPP), ανακοίνωσε η εταιρεία. “Οι εξάρσεις της γενικευμένης φλυκταινώδους ψωρίασης GPP μπορούν να επηρεάσουν σημαντικά τη ζωή ενός ασθενούς και να οδηγήσουν σε σοβαρές, απειλητικές για τη ζωή επιπλοκές”, δήλωσε ο Mark Lebwohl, MD, κύριος ερευνητής στην κεντρική μελέτη της σπεσολιμάμπης, σε δελτίο τύπου της εταιρείας.
“Η έγκριση του Spevigo αποτελεί σημείο καμπής για τους δερματολόγους και τους κλινικούς γιατρούς. Διαθέτουμε πλέον μια εγκεκριμένη από τον FDA θεραπεία που μπορεί να βοηθήσει να κάνουμε τη διαφορά για τους ασθενείς μας, οι οποίοι, μέχρι τώρα, δεν είχαν καμία εγκεκριμένη επιλογή για να βοηθήσουν στη διαχείριση των εξάρσεων της γενικευμένης φλυκταινώδους ψωρίασης GPP”, δήλωσε ο Lebwohl, κοσμήτορας για την κλινική θεραπευτική και καθηγητής δερματολογίας, στη Σχολή Ιατρικής Icahn στο Mount Sinai, στη Νέα Υόρκη.
Η σπεσολιμάμπη είναι ένα νέο, επιλεκτικό μονοκλωνικό αντίσωμα που εμποδίζει τη σηματοδότηση της ιντερλευκίνης-36, η οποία είναι γνωστό ότι εμπλέκεται στην γενικευμένη φλυκταινώδη ψωρίαση GPP. Έλαβε αξιολόγηση κατά προτεραιότητα και είχε χαρακτηρισμό ορφανού φαρμάκου και πρωτοποριακής θεραπείας.
Η γενικευμένη φλυκταινώδης ψωρίαση GPP προσβάλλει περίπου 1 στους 10.000 ανθρώπους στις ΗΠΑ.
Αν και σπάνια, η γενικευμένη φλυκταινώδης ψωρίαση GPP είναι μια δυνητικά απειλητική για τη ζωή νόσος που διαφέρει από την ψωρίαση κατά πλάκας. Η γενικευμένη φλυκταινώδης ψωρίαση GPP προκαλείται από τη συσσώρευση ουδετερόφιλων στο δέρμα.
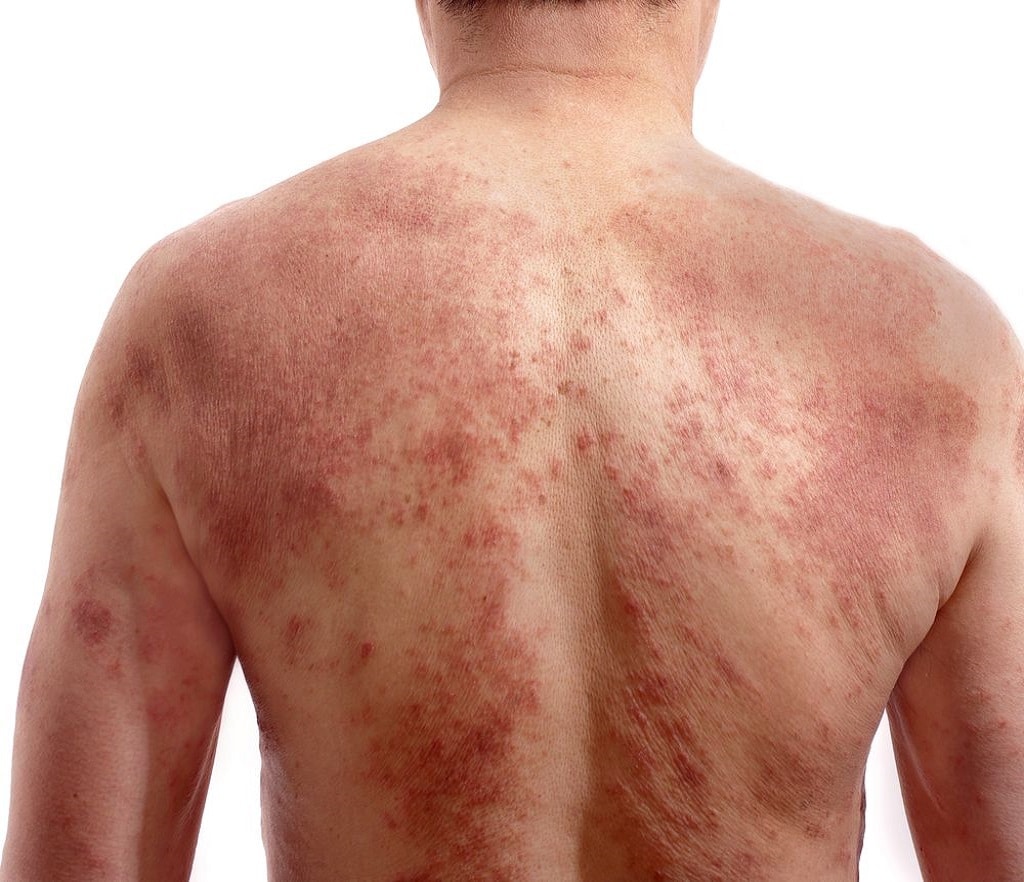
Κατά τη διάρκεια της πορείας της νόσου, οι ασθενείς μπορεί να υποφέρουν από επαναλαμβανόμενα επεισόδια εκτεταμένων εξάρσεων επώδυνων, στείρων φλυκταινών σε όλα τα μέρη του σώματος.
Η σπεσολιμάμπη αξιολογήθηκε σε μια συνολική κλινική δοκιμή 12 εβδομάδων, ελεγχόμενη με εικονικό φάρμακο, στην οποία συμμετείχαν 53 ενήλικες που αντιμετώπιζαν έξαρση της γενικευμένης φλυκταινώδους ψωρίασης GPP. Μετά από 1 εβδομάδα, σημαντικά περισσότεροι ασθενείς που έλαβαν θεραπεία με spesolimab σε σχέση με το εικονικό φάρμακο δεν εμφάνισαν ορατές φλύκταινες (54% έναντι 6%), σύμφωνα με την εταιρεία.
Οι πιο συχνές ανεπιθύμητες ενέργειες, που παρατηρήθηκαν σε τουλάχιστον 5% των ασθενών που έλαβαν θεραπεία με σπεσολιμάμπη, ήταν ασθένεια και κόπωση, ναυτία και έμετος, πονοκέφαλος, κνησμός και κνησμός, αιμάτωμα και μώλωπες στο σημείο έγχυσης και λοίμωξη του ουροποιητικού συστήματος.
Οι πλήρεις πληροφορίες συνταγογράφησης και ένας οδηγός φαρμακευτικής αγωγής είναι διαθέσιμα στο διαδίκτυο.